Periodensystem
Periodensystem
Das Periodensystem dient zur Klassifizierung von Elementen nach ihren Ähnlichkeiten in den chemischen und physikalischen Eigenschaften. In dieser Tabelle sind die Elemente in aufsteigender Ordnungszahl angeordnet. Die allgemeine Form des Periodensystems ist unten angegeben. 
Im Periodensystem sehen Sie Ordnungszahl, Name, Symbol und Massenzahl der Elemente. Wie Sie dem obigen Bild entnehmen können, werden horizontale Zeilen als Periode und vertikale Spalten als Gruppe bezeichnet. Im Periodensystem gibt es 7 Perioden und zwei Gruppen A und B. Die Gruppen A und B haben ebenfalls 8 Untergruppen (8B hat drei Spalten). In einer Periode ändern sich die Eigenschaften von Elementen von links nach rechts. In einer Gruppe haben Elemente ähnliche chemische Eigenschaften.
Orbitale im Periodensystem
s-Block: Dieser Block enthält Elemente mit Valenzelektronen im s Orbital. IA und IIA sind s Blockgruppen. Zum Beispiel,
1s22s22p63s1 und 1s22s2 sind s Blockelemente.
p-Block: Dieser Block enthält Elemente mit Valenzelektronen in p-Orbitalen. IIIA, IVA, VA, VIA, VIIA und VIIIA sind p-Blockgruppen. Zum Beispiel,
1s22s22p63s23p5und 1s22s22p63s23p64s23d104p3 sind p-Blockelemente.
d-Block: Dieser Block enthält Elemente mit Valenzelektronen in d-Orbitalen. IIIB, IVB, VB, VIB, VIIB, VIIIB, IB und IIB sind d-Blockgruppen. Zwei Elemente links unten gehören nicht zum Block d. Zum Beispiel,
1s22s22p63s23p64s23d4 und 1s22s22p63s23p64s23d10 sind d-Blockelemente.
d Blockelemente werden auch Übergangselemente genannt und sind alle aus Metall.
f-Block: Dieser Block enthält Elemente mit Valenzelektronen in f-Orbitalen. Zwei in d-Block (IIIB) erwähnte Elemente und zwei am Ende des Periodensystems gezeichnete Zeilen gehören zu f-Block.
1s22s22p63s23p64s23d104p65s24d105p66s24f3 ist ein Beispiel für ein f-Block-Element.
f Blockelemente werden auch als innere Übergangselemente bezeichnet. Sie sind in zwei Gruppen Lanthanoide und Actinoide unterteilt.
Das folgende Periodensystem zeigt Blöcke im Detail. 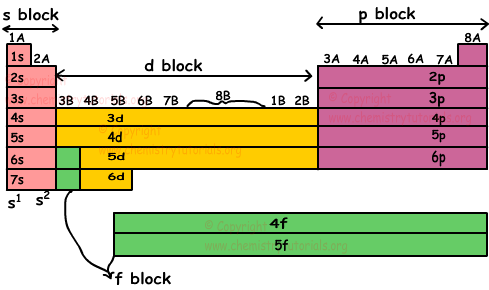
Lanthanoide sind Elemente mit einer Ordnungszahl zwischen 58 und 71. Actinoide sind Elemente mit einer Ordnungszahl zwischen 90 und 103.
s- und p-Blöcke werden als Hauptgruppen bezeichnet. Die folgende Liste zeigt einige wichtige Gruppennamen.
IA = Alkalimetalle
IIA = Alkalische Erden
VIIA = Halogene
VIII = Edelgase