Messung von Enthalpie und Kalorimeter
Messung von Enthalpie und Kalorimeter
Der größte Teil der Enthalpieänderung kann experimentell gemessen werden. Dieser Vorgang wird als “Messung der Wärmeübertragung” -Kalorimetrie bezeichnet. Kalorimeter sind Geräte zur Messung des Wärmestroms. In Kalorimetern;
Wärmeaufnahme = Wärmeabgabe
Ein einfaches Kalorimeter ist in der folgenden Abbildung dargestellt. 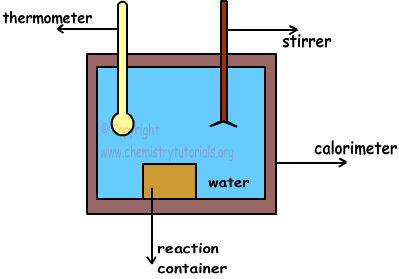
Das Kalorimeter ist ein mit Wasser gefüllter und isolierter Behälter. Da es isoliert ist, geht keine Wärme verloren und es erfolgt keine Übertragung mit der Umgebung. Angelegenheiten werden in den Reaktionsbehälter gegeben. Mit Hilfe des Rührers stellen wir die Wassertemperatur überall gleich ein. Darüber hinaus wird ein Thermometer verwendet, um die Wassertemperatur vor und nach Beendigung der Reaktion zu messen.
Ti = Anfangstemperatur (vor der Reaktion)
Tf = Endtemperatur (nach der Reaktion)
Nach Messungen wenn;
Die Reaktion Ti <Tf gibt Wärme an Wasser und erhöht dessen Temperatur. Somit ist es eine exotherme Reaktion.
Ti> Tf, die Reaktion absorbiert Wärme aus dem Wasser und senkt die Temperatur. Somit ist es eine endotherme Reaktion.
Der Wärmefluss im Kalorimeter wird mit der folgenden Formel berechnet:
Q=mcal.ccal.∆T + mwasser. cwasser.∆T
Wo;
mcal= Masse des Kalorimeters in g
ccal=spezifische Wärmekapazität des Kalorimeters
mwasser= Wassermasse in g.
cwasser= spezifische Wärmekapazität von Wasser
∆T = Differenz zwischen Anfangs- und Endtemperatur
Da ∆T für Wasser und Kalorimeter gleich ist, wird die Formel; Q=(mcal .ccal + mwasser + cwasser).∆T
Wenn wir schreiben;
Ccal=mcal.ccal
Cwasser=mwasser.cwasser
Q=(Ccal + Cwasser). ∆T=Csystem.∆T
Wir kennen die Molzahl der Reaktanten. Je nach Reaktionskoeffizient wird der ∆H-Wert berechnet. Wenn die Temperatur des Systems ansteigt, ist die Reaktion endotherm und wir nehmen ∆H positiv an. Wenn die Temperatur des Systems ansteigt, ist die Reaktion exotherm und ∆H wird negativ.
Beispiel: Welche der folgenden Anwendungen sind exotherm?
I. X (g) + Y (g) → Z (g) + T (g)
Die Summe der Bindungsenergien der Produkte ist größer als die Summe der Bindungsenergien der Reaktanten.
II. Wenn sich Verbindung A in Wasser löst, nimmt die Wassertemperatur ab.
III. 2B(g) + C(g) → 2D(g)
Die oben angegebene Reaktion findet in einem isolierten Behälter statt und der Druck in dem Behälter steigt an.
Lösung:
I. Wenn die Summe der Bindungsenergien der Produkte größer ist als die Bindungsenergien der Reaktanten, ist die Energie, die durch die Bildung einer neuen Bindung in den Produkten freigesetzt wird, größer als die Energie, die zum Aufbrechen der Bindungen der Reaktanten verwendet wird. Mit anderen Worten ist die Reaktion exotherm.
II. Wenn die Wassertemperatur abnimmt, absorbiert die Reaktion Wärme aus dem Wasser. Somit ist die Reaktion endotherm.
III. Bei dieser Reaktion nehmen die Mol Gase ab, im Gegenteil, der Druck steigt an. Um den Druck zu erhöhen, erhöht sich auch die Temperatur des Systems. Die Reaktion muss also exotherm sein.
Beispiel: Die Verbrennungsenthalpie von Kohle beträgt 5500 kcal / g. Um 5 kg Wasser im Kalorimeter von 20 ° C auf 42 ° C zu erhöhen, wie viele kg Kohle müssen verbrannt werden? (cwasser= 1cal / g 0c)
Lösung:
Die zum Erhöhen der Temperatur von 5 kg = 5000 g Wasser von 20 ° C auf 42 ° C erforderliche Wärme wird mit der folgenden Formel berechnet: Q= m.c.∆T
Q=5000.1.(42-20)
Q=110000 cal
Bei Verbrennung von 1 g Kohle werden 5500 cal Wärme freigesetzt
Bei Verbrennung von X g Kohle werden 110000 cal Wärme freigesetzt —————————————————————–
X=20 g coal
Die Enthalpie der Reaktionen hängt ab von;
- Menge der Materie
- Physikalischer Zustand der Materie
- Druck
- Temperatur
- Arten von Materie