Кинетическая теория газов
Кинетическая теория газов
Кинетическая теория - это модель, которая касается движения атомов / молекул газа в закрытом контейнере. * Молекулы или атомы газа совершают случайные движения в контейнере.
- Во время этого случайного движения они сталкиваются друг с другом и поверхностью контейнера.

- Они равномерно диффундируют в контейнере. Если мы поместим два разных газа в один контейнер, они образуют однородную смесь.
- Пространства между молекулами и атомами в газах больше, чем пространства между частицами в твердых телах и жидкостях.
- В одно мгновение скорости атомов / молекул газа не равны. Они обратно пропорциональны квадратному корню из молекулярной массы и прямо пропорциональны квадратному корню из абсолютной температуры.
- При одинаковой температуре средние кинетические энергии всех атомов / молекул равны.
- Столкновения атомов / молекул газа друг с другом и поверхностью контейнера являются упругими, поэтому энергия не теряется.
- Притяжение между атомами / молекулами газа слабое.
Все приведенные выше свойства принадлежат идеальному газу. Тем не менее, нет такого газа, подчиняющегося этим правилам. Газ должен иметь низкое давление и молярную массу, а также большой объем и температуру, чтобы стать идеальным газом. Если газы сжимаются (повышение давления, снижение температуры), они конденсируются.
Пример: какое из следующих утверждений, касающихся газов, является ложным.
I. Они могут производить гомогенные смеси.
II. Плотность того же вещества в газовой фазе меньше плотности жидкой фазы.
III. Они текучие.
III. Они прикладывают одинаковое давление в каждой точке контейнера.
V. Они могут конденсироваться при низком давлении и высокой температуре.
Все утверждения верны, кроме V. Это должно быть;
Газы конденсируются под высоким давлением и низкой температурой.
Пример: Какие из следующих утверждений верны в отношении данных газов при тех же условиях. 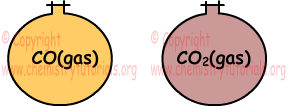
I. Давление газов возникает в результате столкновения атомов / молекул друг с другом.
II. Оба газа имеют одинаковую среднюю кинетическую энергию.
III. Количество молекул, сталкивающихся с единичной поверхностью в единицу времени в первом контейнере, больше, чем во втором контейнере.
Решение:
Давление газа возникает в результате столкновения частиц с поверхностью контейнера. Таким образом, I. ложно
II и III правда.