Химическое равновесие
Химическое равновесие
До сих пор мы узнали, что реакции происходят в одном направлении. Но сейчас мы имеем дело с обратимыми реакциями. Реакция, приведенная ниже, находится в закрытом контейнере; A(g) + B(g) → C(g) + D(g)
В начале А реагирует с В и образует газы С и D. Это «прямая реакция », и скорость этой реакции записывается как;
Скорость реакции = kf. [A]. [B]
Поскольку концентрации A и B со временем уменьшаются, скорость прямой реакции также уменьшается. Кроме того, полученные молекулы C и D сталкиваются друг с другом и образуют молекулы A и B. Это называется «обратной реакцией », а скорость ее написана как;
Скорость реакции = kr. [C]. [D]
Концентрация газов C и D увеличивается, а A и B уменьшается со временем. В какой-то момент скорости реакции прямой и обратной реакции становятся равными, и реакция достигает равновесия. Мы пишем это уравнение как;
kf.[A].[B] = kr.[C].[D]
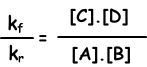
kf / kr = константа равновесия и представлена с помощью Kc в виде концентрации. Константа равновесия следующей реакции записывается в виде;
aA + bB ↔ cC + dD
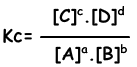
Уравнение равновесия записывается из общей реакции. Мы не касаемся шагов реакций, как в случае однонаправленных реакций. Реакции должны подчиняться следующим правилам, чтобы достичь равновесия;
- Система должна быть закрыта
- Температура должна быть постоянной
- Реакция должна быть обратимой
Если температура изменяется, то скорость реакции прямого или обратного хода может быть изменена, и система не достигнет равновесия. Если реакция необратима, мы не можем говорить о равновесии. Наконец, закрытые системы необходимы для предотвращения потери вещества во время реакции. Теперь мы узнаем, почему системы стремятся достичь равновесия.
- Все системы хотят уменьшить свою энергию. Это тенденция минимальной энергии.
- Все системы имеют тенденцию увеличивать их беспорядок. Это называется тенденцией максимального беспорядка.
Вода в открытом контейнере со временем испаряется. Жидкая вода имеет меньшую энергию, чем газовая вода, и подчиняется закону минимальной энергии. Напротив, его испарение можно объяснить законом максимального беспорядка. Молекулы жидкой воды изменяют свою фазу на газ и увеличивают беспорядок.
Расстройство;
Газ> Решения> Жидкость> Твердое вещество
Энергия;
Газ> Жидкость> Твердое вещество
P.S:
Растворение твердых веществ и жидкостей является экзотермическим или эндотермическим. Однако растворение газов всегда экзотермично.
Пример: Какие из следующих реакций могут быть экзотермическими?
I. 2HI(g) ↔ H2(g) + I2(g)
II. 2NH3(g) ↔ N2(g) + 3H2(g)
III. CO2(g) ↔ CO2(aq)
IV. CaCO3(s) ↔ CaO(s) + CO2(g)
V. N2O4(g) ↔ 2NO2(g)
Решение: все реакции I, II и V находятся в газовой фазе. Беспорядок увеличивается в направлении продуктов. Итак, эти реакции являются эндотермическими. В реакции IV твердое вещество меняет фазу и становится газом. Поскольку беспорядок увеличивается от твердой до газовой фазы, эта реакция является эндотермической. В реакции III беспорядок увеличивается от продуктов к реагентам, и реакция является экзотермической.
Гомогенное и гетерогенное равновесие
Если все вещества в равновесной реакции находятся в одной фазе, то это гомогенное равновесие, если хотя бы одно из веществ имеет другую фазу, то это гетерогенное равновесие.
Когда мы пишем уравнение равновесия гетерогенного равновесия, мы не пишем чисто твердые и чисто жидкие вещества в уравнении равновесия. Например;
2NH3(g) ↔ N2(g) + 3H2(g)
реакция является однородной реакцией, и мы записываем все вопросы в уравнение равновесия.
CaCO3(s) ↔ CaO(s) + CO2(g)
Эта реакция является гетерогенной равновесной реакцией, и мы не записываем CaCO3 (s) и CaO (s) в уравнение равновесия.
Константа равновесия в терминах парциального давления
Концентрации газов прямо пропорциональны парциальному давлению их. Таким образом, мы можем записать константу равновесия в терминах парциальных давлений.
N2(g) + 3H2(g) ↔ 2NH3(g)
Константа равновесия этой реакции в пересчете на концентрации равна;
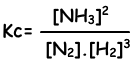
Константа равновесия этой реакции по парциальному давлению равна;
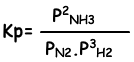
Отношение между этими двумя константами равновесия есть;
Kp=Kc(R.T)∆n
∆n = ∑n (реагенты) - ∑n (продукты)
Например: N2(g) + 3H2(g) ↔ 2NH3(g)
Поскольку ∆n (продукты) = 2 (2 моль NH3) и ∆n (реагенты) = 4 (1 моль N2 и 3 моль H2)
∆n= -2
Kp=Kc.(R.T)-2