Атомная структура с примерами
Атомная структура с примерами
Атом - самая маленькая частица материи. Он состоит из трех частиц, называемых протоном, электроном и нейтроном. Протоны и нейтроны расположены в центре атома, а электроны - вокруг центра. На рисунке ниже показана структура атома и расположение протона нейтрона и электрона в атоме. 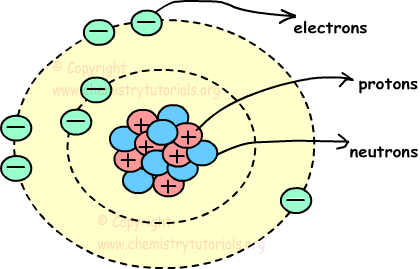
Центр атома, включая протоны и нейтроны, называется также ядром, а окружности вокруг ядра называются орбитами.
Протоны: Протоны - это положительно заряженные частицы атомов. Они расположены в ядре и имеют массу. Мы показываем протоны с буквой «р».
Электроны: Электроны - это отрицательно заряженные движущиеся частицы атомов. Они расположены вокруг ядра на орбитах и не имеют массы. Мы показываем электроны с буквой «е».
Нейтроны: Нейтроны являются бесплатными частицами атомов. Они расположены в ядре и имеют массу. Мы показываем нейтроны с буквой «п». 
Атомный номер:
Атомный номер показывает количество протонов в каждом атоме. Он специфичен для каждого атома и обозначен буквой «Z». В нейтральном атоме число протонов равно числу электронов. Таким образом,
Z=p=e
Атомный номер записывается как;
атомный номерX
Массовое число:
Масса нейтрона примерно равна массе протона. Мы пренебрегаем массой электрона, так как он слишком мал. Таким образом, масса атома равна сумме массы протонов и нейтронов. Показываем массовое число буквой “М”. Массовое число не является специфическим для каждого атома. Разные атомы могут иметь одинаковое массовое число.
M=n+p
Мы показываем «М» на атоме как;
ZMX
Изотопы:
Изотопы имеют одинаковый атомный номер, но разные массовые числа. Это означает, что атомы имеют одинаковое количество протонов, но разное количество нейтронов. Поскольку число протонов одинаково, химические свойства атомов одинаковы, а поскольку число нейтронов различно, физические свойства атомов различны. Изотопы водорода приведены ниже;
11H,
12H ,
13H
изотоны:
Атомы изотона имеют одинаковое количество нейтронов и разное количество протонов.
Натрий и магний являются изотонными атомами, их число нейтронов одинаково.
1123Na и 1224Mg
Изобары:
Атомы изобары имеют разные атомные номера и разные нейтронные числа, но одинаковые массовые числа. 1124Na и 1224Mg
Поскольку число протонов и число нейтронов атомов различны, их физические и химические свойства также различны.
Пример: какое из следующих утверждений одинаково для атомов изотопов
I. Количество протонов
II. Количество нейтронов
III. Количество электронов
IV. Атомный номер
V. Химические свойства
VI. Физические свойства
Изотопы имеют одинаковый атомный номер, но разные массовые числа. Это означает, что атомы изотопов имеют одинаковое количество протонов и разное количество нейтронов. Если атом нейтрален, то число протонов в атоме равно числу электронов. Поскольку число протонов атомов одинаково, а число нейтронов различно; химические свойства этих атомов одинаковы, но физические свойства их различны. Таким образом,
I. III. IV. и V верно для атомов изотопов.
Пример: Найти число протонов атома, имеющих массовое число 65 и нейтронное число 35.
Массовое число равно сумме протонов и нейтронов.
M=p+n
65=35+p
p=30
Пример: Какие из следующих утверждений верны для 1224X и 1124Y атомов.
I. Количество протонов X> Y
II. нейтронное число Y больше нейтронного числа X
III. Их массовые числа равны
1224X :
Х имеет 12 протонов и
24-12=12 нейтроны
Массовое число = 24
1124Y:
Y имеет 11 протонов и
24-11 = 13 нейтронов
Массовое число = 24
Таким образом, I. II. и III. это правда.
Пример: I. 2656Fe+2, 2656Fe+3
II. 2656Fe, 2756Co
III. H2O, D2O
Какая из пар приведенных выше имеет одинаковые химические свойства.
(11H, 12D)
Чтобы иметь одинаковые химические свойства, они должны иметь одинаковое количество протонов и электронов.
I. У них обоих одинаковые числа протонов 26, но их электронные числа разные. Первый имеет 26-2 = 24 электрона, а второй 26-3 = 23 электрона. Таким образом, они имеют разные химические свойства.
II. Поскольку оба они имеют разное количество протонов и электронов, они имеют разные химические свойства.
III. В этой паре у них одинаковое количество протонов и электронов, они имеют одинаковые химические свойства.