Фазы (состояния) материи с примерами
Фазы (состояния) материи с примерами
Вопросы могут существовать в четырех штатах; твердое тело, жидкость, газ и плазма. Некоторые специфические свойства этих фаз показаны в таблице ниже. 
В этом разделе мы рассмотрим твердые вещества, жидкости и газы. Форма, приведенная ниже, обобщает фазовые изменения веществ от твердого к жидкому, от жидкого к газу
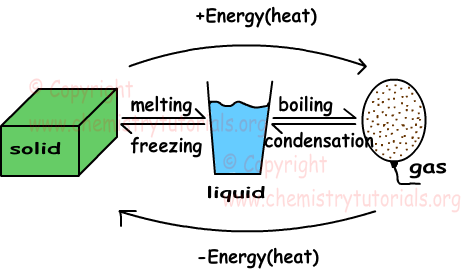
Когда мы даем тепло материи в три фазы, она увеличивает среднюю кинетическую энергию частиц. Для того же вещества кинетическая энергия частиц в газовой фазе больше кинетической энергии в твердом и жидком состояниях. Определения некоторых понятий, связанных с фазовым переходом, приведены ниже.
Таяние: твердое тело изменяет свое состояние в жидкость.
Замораживание: обратный процесс плавления называется замерзанием. Жидкое вещество теряет тепло и меняет свое состояние на твердое.
Кипение: жидкие вещества нагреваются и меняют свое состояние на газ
Конденсация: обратный процесс кипения называется конденсацией. Молекулы газа теряют тепло и меняют свою фазу на жидкость.
Во время фазовых изменений температура вещества остается постоянной. Графики фазовых изменений приведены ниже.
График зависимости температуры от времени нагреваемого чистого твердого вещества приведен ниже. 
В промежутках I. III. и В. температура вещества увеличивается. Поскольку вещество является чистым, его кинетическая энергия также увеличивается. Мы можем найти тепло, полученное в этих интервалах, по следующей формуле;
Q = m.c.ΔT
где; m - масса, c - удельная теплоемкость, а ΔT - изменение температуры (Tfinal-Tinitial).
В промежутках II. и IV. температура вещества остается постоянной, потому что вещество меняет фазу. Поскольку температура вещества постоянна, его кинетическая энергия также постоянна. Напротив, при смене фазы расстояния между молекулами увеличиваются, поэтому потенциальная энергия вещества также увеличивается. В этих интервалах мы имеем гетерогенные смеси, например, в интервале II. мы имеем твердую + жидкую смесь и в интервале IV. у нас есть смесь жидкость + газ. Мы находим тепло, требуемое в этих интервалах, по следующим формулам;
Q=m.Lfusion или же Q=m.Lvaporization
где m - масса, «L-синтез» - скрытая теплота плавления, а «L-испарение» - скрытая теплота испарения.
Потеря тепла вещества в газовой фазе имеет график зависимости температуры от времени, как показано ниже. 
Как вы можете видеть на обоих графиках, точка кипения становится точкой конденсации, а точка плавления становится точкой замерзания в процессе охлаждения. Их величины равны. Мы используем те же формулы, что и выше, чтобы найти тепло, выделяемое веществом во время этого процесса.
Мы решаем несколько примеров, связанных с изменением фазы.
Пример: Найти тепло, необходимое для повышения температуры 100 г льда с 00C до 40 ° С (вода = 1 кал / г ° С, Lслияние = 80 кал / г)
Решение:
Сначала мы растопим лед, а затем нагреем его до 40 ° С.
Q1=m.Lслияние
Q1=100g.80.cal/g
Q1=8000 cal
Сейчас мы повышаем температуру от 0 до 40 ° С.
Q2=m.c.ΔT
Q2=100.1.(40-0)
Q2=4000cal
Qtotal=Q1+Q2=8000cal+4000cal=12000cal.
Пример: если мы смешаем две воды, имеющие массу 150 г, температуру 40 ° С, 100 г и 80 ° С, определим конечную температуру смесей (вода = 1 кал / г ° С).
Решение:
Когда два вещества, имеющие разные температуры, находятся в контакте, между ними происходит теплообмен. Тепло течет от вещества, имеющего более высокую температуру, к веществу, имеющему низкую температуру, пока они не получат равные температуры. Полученное тепло всегда равно потерянному теплу. 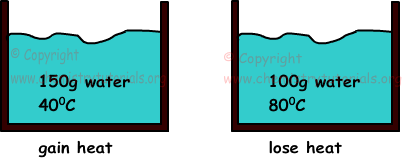
температура конечной смеси должна быть между температурами обеих вод
400C<Tfinal<800C
Qполучили=Qпотерянный
m1.c1.ΔT1=m2.c2.ΔT2
150.1.(T-40)=100.1.(80-T)
T=560C