Разведение и плотность растворов
Разведение и плотность растворов
Разбавление - это процесс добавления растворителя в раствор. Поскольку количество растворенного вещества остается постоянным, концентрация раствора уменьшается. Находим связь между концентрацией растворов до и после разбавления по следующей формуле:
M1.V1=M2.V2
Где M1 - начальная молярность, а M2 - конечная молярность, а V1 и V2 - начальный и конечный объемы раствора.
Чтобы увеличить концентрацию растворов, следует добавить растворенный или выпарить растворитель из раствора. Формула, приведенная выше, также используется для увеличения концентрации растворов;
M1.V1=M2.V2
Концентрация растворов и объемы обратно пропорциональны друг другу. Если объем раствора увеличивается, молярность раствора уменьшается. График, приведенный ниже, показывает это соотношение; 
Пример: если мы добавим 700 мл воды при той же температуре к 0,2-молярному 300-мл раствору, найдите конечную молярную концентрацию этого раствора.
Решение:
M1 = 0,2 моль, V1 = 300 = 0,3 мл
V2 = 300 + 700 = 1000 мл = 1 л M1.V1=M2.V2
0,2.0,3=M2.1
M2 = 0,06 моль
Пример: если мы смешаем растворы, приведенные на рисунке ниже, найдите концентрацию конечного раствора. 
Решение: сумма решений массы один и два дает нам массу окончательного решения
m1+m2= mокончательный
80 + 40 = 120 г
Сумма растворенных масс один и два дает нам массу окончательного растворенного вещества.
(1) mсахар1 + mсахар2=mсахарf
Мы находим массы растворенных веществ;
mсахар1=m1.20/100=80.1/5=16 г
mсахар2=m2.30/100=40.30/100=12 г
mсахарf=mfinal.X/100=120.X/100 г
используем уравнение (1) и решаем для X;
mсахар1 + mсахар2=mсахарf
16 + 12=120.X/100 г
28=12.X/10
X=23,3
Плотность решений
Находим плотность решений по следующей формуле; 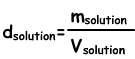
Единица жидких растворов г / мл или г / см3. Вводя растворенное вещество в воду, мы готовим раствор. При добавлении растворенного вещества в раствор его плотность увеличивается, так как увеличение массы раствора больше, чем увеличение объема. В твердых жидких растворах плотность увеличивается с увеличением концентрации раствора.
Пример. Плотность раствора H2SO4 с массовым процентом 49% составляет 1,2 г / мл. Найти молярную концентрацию этого раствора. (H2SO4 = 98)
Решение:
плотность раствора = 1,2 г / мл
Массовый процент = 49%
Молярная масса H2SO4 составляет 98 г.
Найдем молярную концентрацию раствора по следующей формуле: 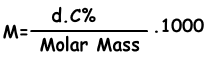
M=(1,2.4)/98 . 1000
М = 6 моль
Пример: Растворимость Х при 15 ° С составляет 20 г Х / 100. Какие из следующих утверждений верны для раствора, приготовленного с использованием 30 г х и 120 г воды при 15 ° С?
I. Раствор насыщен.
II. Масса раствора 150 г.
III. Концентрация в процентах по массе составляет 20%
Решение:
I. при 15 ° С
100 г воды растворяет 20 г х
120 г воды растворяется? г х
¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯
? = 24 г х растворяется.
поскольку 30 г х добавляют к 120 г воды, раствор насыщается, а 30-24 = 6 г х остается нерастворенным. I это правда.
II. Масса раствора равна сумме растворенного вещества и растворителя.
m = m(растворенного вещества) + m(растворителя)
м = 120 + 24 = 144
При этом масса не равна 150 г, II ложно.
III. Поскольку в 100 г воды растворяется 20 г х, в 120 г раствора также содержится 20 г х. Таким образом, проценты по массе;
X% = (мХ / мс растворение) .100
Х% = (20/120) .100 = 16,7
III ложный