Свойства решения и расчеты решения
Свойства решения и расчеты решения
Свойства решений
- Температура кипения, температура замерзания, давление пара и такие свойства, как плотность растворов, отличаются от свойств чистого растворителя. Например, вода кипит при 100 ° С, наоборот, раствор в соленой воде кипит выше 100 ° С.
- Если растворенные в воде вещества не являются летучими, они предотвращают испарение воды, в результате чего температура кипения воды увеличивается, а температура замерзания воды уменьшается. Зимой соль разливают по дороге, чтобы уменьшить температуру замерзания воды.
- В растворе повышение температуры кипения прямо пропорционально молярной концентрации частиц в растворе.
- В жидких растворах уменьшение точек замерзания и давления пара обратно пропорционально молярной концентрации частиц в растворе.
- Проводимость электричества прямо пропорциональна молярной концентрации ионов в растворах. Например, алкоголь и сахар не проводят электричество.
Пример: в следующих баках одинаковое количество воды. Если мы растворяем следующие растворы в этих резервуарах; найти связь между электропроводностью этих растворов.
I. 1 моль NaCl
II. 2 моль сахара
III. 1 моль Al(NO3)3 
Решение:
Электропроводность растворов зависит от молярной концентрации ионов в растворе. Теперь мы находим концентрацию ионов растворов в каждом резервуаре.
I.
NaCl(s) → Na+(aq) + Cl-(aq)
1 моль 1 моль 1 моль
В первом растворе 2 моль иона.
II. Поскольку сахар выполняет молекулярную сольватацию, в растворе нет иона. Таким образом, он не проводит электричество.
III.
Al(NO3)3(s) → Al+3 + 3NO3-1
1 моль 1 моль 3 моль
В этом растворе содержится 4 моля иона.
Объемы растворов равны друг другу, таким образом, возникает связь между электропроводностью растворов; III>I>II
Расчет решений Пример: если мы приготовим 3 раствора под давлением 1 атм, используя 1 л воды и 0,1 моль NaCl, 0,2 моль NaCl, 0,3 моль NaCl для каждого раствора, сравните температуру кипения, температуру замерзания и давление паров этих растворов. 
Решение:
NaCl(s) → Na+(aq) + Cl-(aq)
1 моль NaCl дает 1 моль Na+ и 1 моль Cl- всего 2 моль ионов.
В первом контейнере; 0,1 NaCl дает 0,2 моль иона
Во втором контейнере; 0,2 NaCl дает 0,4 моль иона
В третьем контейнере; 0,3 NaCl дает 0,6 моль иона
Точки кипения растворов связаны с количеством растворенного вещества в растворе. Увеличение количества растворенного вещества увеличивает температуру кипения раствора. Связь между точками кипения раствора; III>II>I
Если температура кипения раствора высокая, то давление его пара низкое. Таким образом, связь между давлениями паров растворов становится;
I> II> III
Если температура кипения раствора высокая, то температура его замерзания низкая. Таким образом связь между точками замерзания решений становится;
I> II> III
Пример: сравнить точки кипения следующих растворов;
I. Ненасыщенный X твердо-водный раствор
II. Насыщенный X твердо-водный раствор
III. Пересыщенный X твердо-водный раствор
Решение:
По мере увеличения количества растворенного вещества в растворе температура кипения также увеличивается. Таким образом, у III есть самое большое растворенное вещество в этом тогда II и наконец I. Связь между ними становится;
III> II> I
Пример: приведенные ниже контейнеры включают растворы при той же температуре и давлении. Если молярная концентрация иона K+ в обоих контейнерах одинакова, какие из следующих утверждений верны для этих растворов?
I. Количество молей растворенных веществ равно.
II. Давление пара в первом контейнере выше, чем во втором контейнере.
III. Температура кипения первого раствора ниже, чем у второго раствора.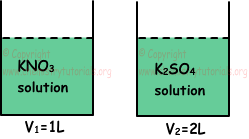
Решение:
Предположим, что молярная концентрация [K+] = 2 М;
I.
1 моль KNO3 включает в себя 1 моль K+, поэтому 2 М K+ иона поступает из 2 М KNO3.
1 моль K2SO4 включает в себя 2 моль K+, поэтому 2 M K+ иона поступает из 1 М K2SO4. Таким образом, моли растворенных KNO3 и K2SO4;
nKNO3=V1.M1=1.2=2 моль
nK2SO4=V2.M2=2.1=2 моль
Итак, число молей растворенных веществ равно I. правда.
II. 2 М KNO3 дает 4 М иона, а 1 М K2SO4 дает 3 М иона. Давление пара обратно пропорционально молярной концентрации частиц в растворе. Таким образом, давление пара второго контейнера выше, чем первого контейнера. II. ложно
III. Температура кипения прямо пропорциональна молярной концентрации частиц в растворе, поэтому раствор в первом контейнере имеет более высокую температуру кипения, чем раствор во втором контейнере. III ложно.