Измерение энтальпии и калориметра
Измерение энтальпии и калориметра
Большая часть изменения энтальпии может быть измерена экспериментально. Этот процесс называется «измерение теплопередачи» калориметрии. Калориметры - это устройства, используемые для измерения теплового потока. В калориметрах;
Тепло поглощается = тепло выпущено
Простой калориметр показан на рисунке ниже; 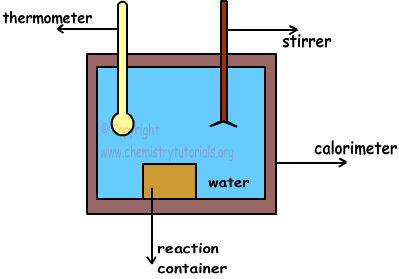
Калориметр представляет собой емкость, наполненную водой и изолированную. Поскольку она изолирована, она не теряет тепло и не передает его окружающим. Вещества помещаются в реакционный контейнер. С помощью мешалки мы делаем температуру воды одинаковой везде. Кроме того, термометр используется для измерения температуры воды до и после завершения реакции.
Ti = начальная температура (до реакции)
Tf = конечная температура (после реакции)
После измерений если;
- Ti <Tf, реакция отдает тепло воде и заставляет ее повышать температуру. Таким образом, это экзотермическая реакция.
- Ti> Tf, реакция поглощает тепло из воды и снижает ее температуру. Таким образом, это эндотермическая реакция.
Тепловой поток в калориметре рассчитывается по следующей формуле:
Q=mcal.ccal.∆T + mwater. cwater.∆T
Где;
mcal= масса калориметра, в г
ccal = удельная теплоемкость калориметра
mwater = масса воды в г
cwater = удельная теплоемкость воды
∆T = разница между начальной и конечной температурой
Поскольку ∆T одинаков для воды и калориметра, формула становится;
Q=(mcal .ccal + mwater + cwater). ∆T
Если мы напишем;
Ccal=mcal.ccal
Cwater=mwater.cwater
Q=(Ccal + Cwater).
∆T=Csystem.∆T
Мы знаем количество молей реагентов. По коэффициенту реагирующих веществ рассчитывается значение ΔH. Если тогда температура системы возрастает, реакция эндотермична, мы принимаем ΔH положительным. Если температура системы возрастает, то реакция экзотермическая и ∆H становится отрицательной.
Пример: Какие из следующих приложений являются экзотермическими?
I. X(g) + Y(g) → Z(g) + T(g)
Сумма энергий связи продуктов больше, чем сумма энергий связи реагентов.
II. Когда соединение А растворяется в воде, температура воды снижается.
III. 2B(g) + C(g) → 2D(g)
Реакция, приведенная выше, происходит в изолированном контейнере, и давление в контейнере увеличивается.
Решение:
I. Если сумма энергий связи продуктов больше, чем энергии связи реагентов, энергия, выделяемая при образовании новой связи в продуктах, больше, чем энергия, используемая для разрыва связей реагентов. Другими словами, реакция экзотермическая.
II. Если температура воды снижается, то реакция поглощает тепло из воды. Таким образом, реакция является эндотермической.
III. В этой реакции количество молей газов уменьшается, а давление увеличивается. Чтобы увеличить давление, температура системы также увеличивается. Итак, реакция должна быть экзотермической.
Пример: энтальпия горения угля составляет -5500 ккал / г. Чтобы увеличить 5 кг воды в калориметре с 20 ° С до 42 ° С, сколько кг угля необходимо сжечь? (вода = 1 кал / г 0с)
Решение:
Тепло, необходимое для повышения температуры 5 кг = 5000 г воды с 20 ° С до 42 ° С, рассчитывается по следующей формуле; Q= m.c.∆T
Q=5000.1.(42-20)
Q=110000 cal
При сжигании 1 г угля выделяется 5500 кал.
При сжигании X г угля выделяется 110000 кал.
¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯
Х = 20 г угля
Энтальпия реакций зависит от;
- Количество вещества
- Физическое состояние материи
- давление
- температура
- Типы материи